پیش از هر چیز باید ابتدا به بررسی خود واکنش جانشانی نوکلئوفیلی بپردازیم. همانطور که می دانید، یک واکنش جانشانی، واکنشی است که طی آن یک گروه عاملی به جای گروه عاملی دیگر قرار می گیرد. این جانشانی می تواند به روش های مختلف و با مکانیسم های متفاوتی پیش رود.
یکی از این روش ها، جانشانی از نوع است. به طور کلی، در این واکنش، در یک مرحله، گروه جانشین شونده و گروه ترک کننده با هم عوض می شوند و مولکول سوبسترا دچار وارونگی می شود. در ادامه با جزئیات به تشریح این فرآند می پردازیم.
واکنش جانشانی نوکلئوفیلی چگونه انجام می شود؟
ابتدا باید در مورد تعاریفی که نیاز داریم به اشتراک برسیم:
سوبسترا: مولکولی که جانشانی روی آن اعمال می شود.
گروه ترک کننده: گروهی که توسط یک گروه عاملی دیگر، از سوبسترا کنده می شود و آن را ترک می کند.
هسته دوست: گروه عاملی که روی سوبسترا به جای گروه ترک کننده قرار می گیرد.
فرآیند جانشانی چگونه انجام می شود؟
در این فرآیند، هسته دوست با بار منفی یا بار جزئی منفی، به سوبسترا نزدیک می شود. سپس در یک مرحله، پیوند مربوط به هسته دوست با سوبسترا در حال ایجاد شدن بوده و پیوند ترک کننده با سوبسترا در حالت شکستن قرار می گیرد. هیبریداسیون کربن مورد حمله، در یک مرحله از به
تبدیل می شود (در یک لحظه، پنج گروه به کربن متصل است) سپس گروه ترک کننده سوبسترا را ترک می کند و مجددا هیبریداسیون به
تبدیل می شود. طی این فرآیند، یک وارونگی نیز در مولکول اتفاق می افتد.
به مکانیسم انجام این واکنش توجه کنید:
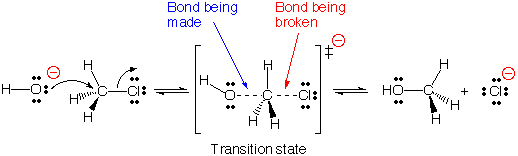
در ادامه به نمودار انرژی بر حسب زمان این نوع واکنش دقت کنید:
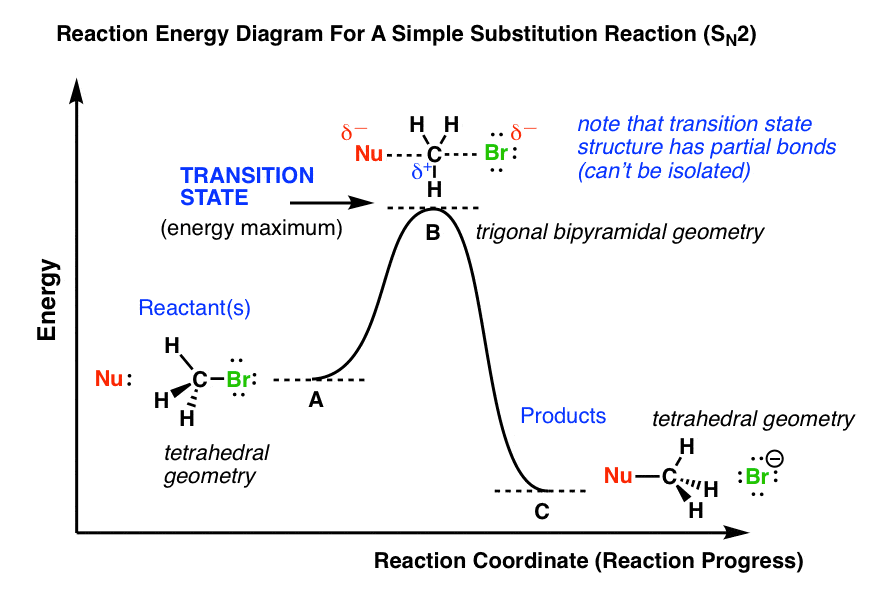
همانطور که مشاهده می کنید؛ حالت گذار این واکنش در یک قله انرژی (نقطه B نمودار) قرار می گیرد و سپس با تجزیه آن، محصول ایجاد می شود. این حالت گذار بسیار ناپایدار بوده و به هیچ عنوان قابل جداسازی نمی باشد. (NU همیشه نماد هسته دوست می باشد.)
ویژگی های جانشانی نوکلئوفیلی :
- این واکنش تک مرحله ای است. یعنی خروج ترک کننده و اتصال هسته دوست، همگی در یک مرحله انجام می شود.
- این واکنش سینتیک مرتبه دو دارد. یعنی در انجام این واکنش، غلظت سوبسترا و هسته دوست، هر دو به یک اندازه اهمیت دارد.
- در این واکنش، پیکربندی مولکول به طور کامل وارونه می شود.
- به علت انجام واکنش در یک مرحله، نوآرایی رخ نمی دهد.
وارونگی پیکربندی رخ می دهد یعنی چه؟
به تصاویر زیر توجه کنید. از بالا به پایین مراحل واکنش جانشانی بین دو مولکول خاص آورده شده است. بین تصویر بالا و پایین، چه تفاوتی می بینید؟ این همان وارونگی پیکربندی است.
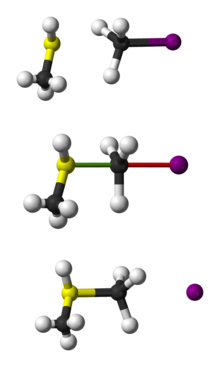
وارونگی پیکر بندی
برای درک بهتر این وارونگی، می تواند وارونه شدن یک چتر را تصور کنید. تصویر زیر گویای این فرآیند است. به آن دقت کنید:

عوامل موثر بر سرعت واکنش های :
1_ نوع آلکیل
هرچه مولکول سوبسترا خلوت تر باشد، سرعت واکنش بیشتر است.
از آنجایی که هسته دوست باید از سمت مخالف گروه ترک کننده به سوبسترا نزدیک شده و به کربن مرکزی آن متصل شود؛ بنابراین هرچه این ناحیه خلوت تر باشد، این واکنش با سرعت بیشتری انجام می شود. در شکل زیر به تغییر سرعت ناشی از تغییر گروه آلکیل توجه کنید:
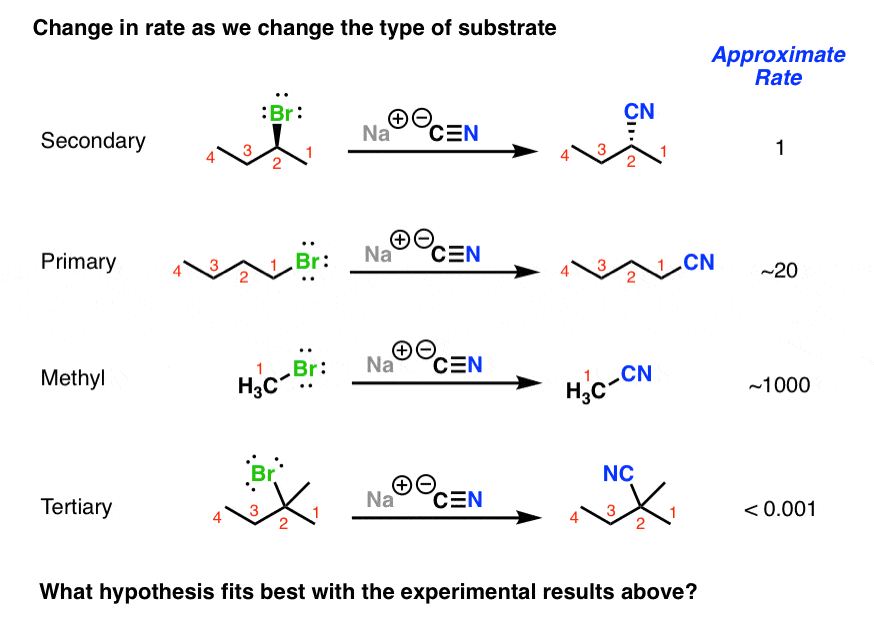
2_ نوع هسته دوست
هرچه هسته دوست قوی تر باشد، سرعت این نوع واکنش بیشتر خواهد بود.
هسته دوست ها اتم یا گروهی از اتم ها هستند که یا بار منفی دارند و یا به طور جزئی دارای بار منفی هستند. این بار منفی جزئی می تواند ناشی از وجود یک زوج الکترون ناپیوندی بوده و یا در اثر یک گروه الکترون کشنده ایجاد شده باشد.
3_ گروه ترک کننده
بهترین ترک کننده آن است که باز بزرگ تر و ضعیف تری باشد. به طور کلی، هر ترک کننده ای که پس از ترک سوبسترا بتواند پایداری بیشتری داشته باشد، ترک کننده بهتری است.
بهترین گروه های ترک کننده درشت مولکول هایی هستند که برای این کار ساخته شده اند و از مهمترین آن ها می توان به گروه تریفیلات، بروسیلات و توسیلات اشاره کرد. به طور کلی، آلکان سولفونات ها ترک کننده های خوبی هستند.
4_ نوع حلال
پیش تر گفتیم که سرعت واکنش زمانی که آلکیل خلوت باشد بالا است. حالا این قضیه را به نوع حلال تعمیم می دهیم. هر چه حلال غیر قطبی تر باشد، امکان حلال پوشی مواد واکنش دهنده، یعنی سوبسترا و هسته دوست کاهش می یابد و بنابراین سرعت واکنش بالا می رود.
عکس این موضوع نیز صادق است. هرچه حلال مورد استفاده، قطبی تر باشد، امکان حلال پوشی مواد درگیر در واکنش بالا رفته و سرعت واکنش را کاهش می دهد.
به این پست چند تا ستاره میدی؟
برای امتیاز دهی روی ستاره ها کلیک کن
امتیاز میانگین 4.5 / 5. تعداد رای ها 2