واکنش هالوژن دار کردن آلکانها
(( بسم الله الرحمن الرحیم))
واکنش هالوژن دار کردن آلکانها
از واکنش هالوژن دار کردن آلکان ها در تهیه گروهی از ترکیبات به نام آلکیل هالیدها استفاده میشود. آلکیل هالیدها آلکان هایی هستند که یک یا چند هیدروژن آنها با هالوژن جایگزین شده است. این واکنش مهم برای تهیه موادی که به عنوان حلال، بیهوش کننده، حشره کش و باکتری کش، مصرف می شوند مورد استفاده قرار می گیرد. در گروهی از واکنش ها پیوندهای شیمیایی در اثر واکنش بین دو جز که هر کدام یک الکترون دارند تشکیل می شوند. هر کدام از این اجزاء (که رادیکال آزاد نامیده میشوند)یک الکترون برای تشکیل پیوند جدید می دهد. همچنین در گسسته شدن پیوند اگر هر جز حاصل از گسستن پیوند یک الکترون داشته باشد گسستن را همولیتیک یا رادیکالی( شکستهشدن جور )می نامند. واکنش های رادیکالی دسته مهمی از واکنشهای عالی هستند. این واکنش ها همچون واکنش های یونی انجام نمیشوند و بررسی آنها اهمیت ویژهای دارد.
اگرچه رادیکالها از نظر الکتریکی خنثی هستند ولی بسیار فعال می باشند زیرا اتم کربن در آنها به جای ۸ الکترون در لایه آخر، ۷ الکترون دارد و مایل است تعداد الکترون های خود را از راه های مختلف به هشت برساند به عنوان مثال رادیکال ،یک اتم از مولکول دیگر می گیرد و در نتیجه رادیکال جدید تشکیل می شود.
°R°+X:Y→R—X+Y
الف)بررسی مکانیسم کلردارشدن متان (رادیکال آزاد)
((کلر دار کردن متان یک واکنش جانشینی رادیکالی است.)) در حالی که آلکانها نسبت به اکثر واکنشگرها از خود واکنشی نشان نمیدهند. در برابر اشعه فرابنفش یا دمای حدود ۴۰۰ درجه سانتیگراد به آسانی با کلر واکنش میدهند و مخلوطی از آلکان های کلر دار به وجود می آورند.
واکنش کلر دار کردن یک واکنش چند مرحلهای است که مراحل آن عبارتند از:
1)مرحله آغاز: شکستن همولیتیک پیوند در کلر
2)مرحله انتشار:
3)مرحله پایان:
معمولاً سه مرحله آغاز انتشار و پایان لازمه انجام واکنشهای رادیکالی است. مرحله آغاز یا شروع واکنش تولید رادیکال فعال است. در این مرحله با تشعشع فرابنفش پیوند ضعیف کلر _کلر می شکند و دو رادیکال فعال کلر ایجاد می شود .پس از تشکیل رادیکال فعال کلر حتی به مقدار بسیار کم پیشرفت واکنشی به طور خود به خودی است .رادیکالهای کلر انرژی زیادی دارند. و بنابراین بسیار فعال هستند این رادیکال ها در برخورد با متان یک اتم هیدروژن از آن می گیرند و HCLو رادیکال متیل تولید می کنند رادیکال متیل حاصل، پر انرژی است و با CL۲ واکنش می دهد در نتیجه کلر و متان و رادیکال کلر تشکیل میشود. رادیکال کلر مرحله اول را دوباره انجام میدهد و بدین صورت فرآیند کلی به صورت یک واکنش زنجیری ادامه مییابد و مراحل الف و ب مرتباً تکرار می شوند.
گاهی ممکن است در اثر برخورد دو رادیکال با یکدیگر و ترکیب آنها با هم محصول های پایداری تشکیل شوند .در چنین حالتی دوره واکنش خاتمه مییابد این چنین واکنش هایی به ندرت انجام می شوند زیرا در هر لحظه غلظت رادیکالها بسیار کم است و در نتیجه احتمال برخورد دو رادیکال نیز بسیار کم میباشد.
به طور کلی کلر دار کردن آلکان ها واکنش سودمندی نیست زیرا بیشتر آلکان ها به استثنای متان و اتان هیدروژن های متفاوتی دارند و محصول عمل معمولا مخلوطی از ترکیبات کلردار است بنابراین در بسیاری از فرآیندهای صنعتی واکنش های زنجیری رادیکالی واکنش های مهم و اساسی می باشند.
نکات زیر در کلردار شدن متان جالب توجه می باشند:
1) متان و کلر در دمای معمولی بر هم اثری ندارند.
2) واکنش کلر دار شدن در دمای بیش از ۲۵۰ درجه سانتیگراد در تاریکی به آسانی صورت می پذیرد.
3) واکنش در اثر اشعه فرابنفش انجام پذیر است.
4) واکنش پس از شروع بسیار سریع و در مواردی حتی انفجاری است.
5) واکنش گرمازا است.
6) نتیجه واکنش محصولات مختلف از قبیل کلرومتان ،دی کلرومتان، تری کلرو متان و تترا کلرو متان و به مقدار کم مواد دیگر است.
7) ((وجود مقدار کمی اکسیژن سرعت واکنش را برای مدتی کم میکند میزان کُند شدن واکنش به مقدار اکسیژن موجود بستگی دارد.))
مراحل زیر در مکانیسم کلردار شدن صورت میگیرند:
آغاز 1) °Cl۲→2Cl
2)Cl°+CH4→HCl+CH3°
انتشار 3) °CH3°+Cl2→CH3Cl+Cl
مراحل 2و 3به دنبال هم تکرار میشوند.
4)2Cl°→Cl__Cl
5)CH3°+CH3°→CH3__CH3
پایان 6) Cl°+CH3°→CH3__Cl
در واکنش کلر دار شدن متان مرحله ۱ که شامل گسسته شدن پیوند مولکول کلر و تشکیل دو اتم کلر است به ۵۸ کیلو کالری برمول انرژی نیاز دارد. این مقدار انرژی از طریق گرما یا نور فرابنفش تامین میشود. اتم کلر بسیار پر انرژی و فعال است که علت آن تمایل این اتم برای به دست آوردن یک الکترون و تشکیل هشتایی است. میدانید لازمه تشکیل پیوند شیمیایی بین دو جز برخورد آنها با یکدیگر است. انرژی سینتیکی دو جز که پیش از برخورد داشته اند ،بعد از برخورد به مقدار حداقلی از انرژی پتانسیل تبدیل می شود.
چون سرعت و در نتیجه انرژی مولکولی تابع دماست، و بنابراین سرعت مولکولها در هر دما توزیع خاصی دارد. تنها مولکول هایی با هم برخورد موثر میکنند که از انرژی سینتیکی کافی برخوردار باشند و مولکولهایی که انرژی سینتیک لازم را ندارند پس از برخورد بدون تشکیل پیوند و انجام واکنش از یکدیگر دور می شوند. مقدار حداقل انرژی لازم برای انجام واکنش تشکیل پیوند شیمیایی را انرژی فعالسازی آن واکنش مینامند .بدیهی است مقدار این انرژی از واکنشی به واکنش دیگر تغییر می کند .از نظر انرژی برخورد اتم کلر با مولکول متان برخوردی محتمل و در جهت تشکیل محصول است.
((اتم یا گروهی از اتم ها را که یک الکترون فرد دارد رادیکال آزاد می نامند))
اثر اکسیژن: در واکنش کلر دار کردن متن مقدار کمی اکسیژن برای مدتی واکنش را کار نمی کند که این مدت به مقدار اکسیژن موجود بستگی دارد پس از مصرف اکسیژن واکنش مجدداً با سرعت عادی پیشرفت می کند به نظر می رسد که اکسیژن با رادیکال متیل ترکیب شده رادیکال جدیدی تولید می کند.
˚CH3°+O2→CH3_O_O
فعالیت رادیکال°CH3—O—O از رادیکالCH3°کمتر است در نتیجه غلظت رادیکال CH3° واکنش مفید بین این رادیکال و Cl—Clکند میشود. پس از آنکه تمام مولکولهای اکسیژن موجود با رادیکال ترکیب شد ،واکنش عادی رادیکال متین با کلر دوباره شروع می شود.
((به این مواد که سبب کند شدن یا متوقف شدن واکنش رادیکالی میشوند کند کننده یا بازدارنده میگویند)) مدت زمانی که تحت تأثیر ماده کند کننده سرعت واکنش رادیکالی کم میشود نیز دوره کندی نامیده می شود .متوقف یا کند شدن واکنش تحت اثر مواد کند کننده راهی برای شناخت و تشخیص واکنش های رادیکالی است.

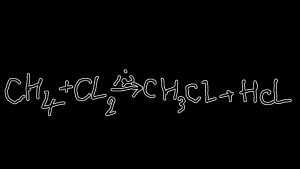
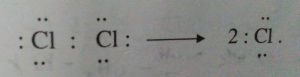

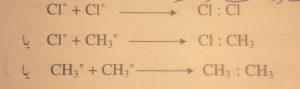



2 دیدگاه در “واکنش هالوژن دار کردن آلکانها”
خدايي صريح و مختصر و مفيد بود حيفم اومد تشكر نكنم
ممنون از لطف شما 🙂