همانطور که می دانید، در شیمی که همه ما می شناسیم، آن چه که وجود دارد، پیوند های مختلف شیمیایی اعم از کوالانسی، یونی و… است. ما بررسی می کنیم که چگونه دو مولکول با هم وارد واکنش شده و یک مولکول جدید می سازند یا اینکه چرا فلان پیوند قوی تر از پیوند دیگر است و…
اما این ها برای شناخت طبیعت کافی نیست. یک مولکول DNA را فرض کنید. ما می دانیم که این ابر مولکول از دو رشته پیچ و تاب خورده تشکیل شده است. اما در عین حال می دانیم که این دو رشته می توانند از هم جدا شوند و یا دوباره به هم متصل شوند (اتفاقی که در همانند سازی DNA رخ می دهد).
این اتصال از نوع پیوند های کوالانسی نیست و صرفا از طریق برهمکنش واندروالسی بسیار قوی به نام پیوند هیدروژنی رخ می دهد (توجه داشته باشید که پیوند هیدروژنی جزو پیوند های شیمیایی قرار نمی گیرد و ما به اشتباه آن را پیوند می نامیم؛ چیزی که ما آن را به عنوان پیوند هیدروژنی می شناسیم، در واقع برهمکنشی غیر پیوندی از نوع واندروالسی است؛ اما چون قدرت آن نسبت به پیوند های کوالانسی کمتر و نسبت به برهمکنش های واندروالسی قوی تر است آن را نه در حوزه پیوند ها و نه در حوزه نیرو های برهمکنشی بررسی می کنیم. بلکه آن را تحت عنوان پیوند هیدروژنی و در دسته ای جداگانه بررسی می کنیم).
حالا باید چه کنیم؟ برای بررسی ابرمولکولی مثل DNA باید به کدام حوزه شیمی مراجعه کنیم؟ سراغ پیوند های کوالانسی برویم یا از برهمکنش های واندروالسی استفاده کنیم؟
البته مثال های دیگری نیز وجود دارد. ابرمولکول های متعددی وجود دارد که نمی توانیم آن ها را در حوزه شیمی کوالانسی یا واندروالسی بررسی کنیم. پس دسته ای جداگانه ایجاد می کنیم تا به طور اختصاصی به این مواد بپردازیم. نام این دسته را سوپرامولکول می گذاریم و با این مقدمه شروع می کنیم.
اما توجه کنید که ما ابرمولکول های متعددی داریم که می توانیم با استفاده از شیمی کوالانسی هم درباره آن ها صحبت کنیم، ابرمولکول هایی مثل الماس، گرافن، MOF ها و… در این دسته قرار می گیرند.
پس هر ابرمولکولی در دسته سوپرا مولکول قرار نمی گیرد. اما وجه تمایز چیست؟ مرز بین یک ابرمولکول و یک سوپرامولکول کجاست؟
سوپرامولکول چیست؟
سوپرامولکول در واقع یک ابرساختار از تجمع مولکول و اتم ها (یا صرفا تجمع مولکول هاست) که در ایجاد و شکل گیری این ساختار، صرفا نیرو های غیر پیوندی دخالت دارد. این نیرو ها می توانند از یونی (با اختلاف الکترونگاتیوی خیلی زیاد)، تا نیرو های کاملا واندروالسی (با کمترین اختلاف الکترونگاتیوی) مختلف باشد.
در ادامه به چند مثال توجه کنید:
این ساختار، مثال خوبی از یک سوپرامولکول است که از دو مولکول با رنگ آبی و قرمز (فعلا به ماهیت این مولکول های رنگی کار نداریم و صرفا قصد معرفی ساختار را داریم) ساخته شده است. در این ساختار، خطوط نشان دهنده پیوند های کوالانسی و نقطه چین ها نشان دهنده پیوند های هیدروژنی است.
مجددا تاکید داریم که پیوند هیدروژنی واقعا پیوند نبوده و یک نوع برهمکنش واندروالسی است که چون قدرت آن خیلی بیشتر از برهمکنش های واندروالسی معمول است، به آن ها عبارت پیوند را نسبت می دهیم؛ در حالی که واقعا پیوندی وجود ندارد.
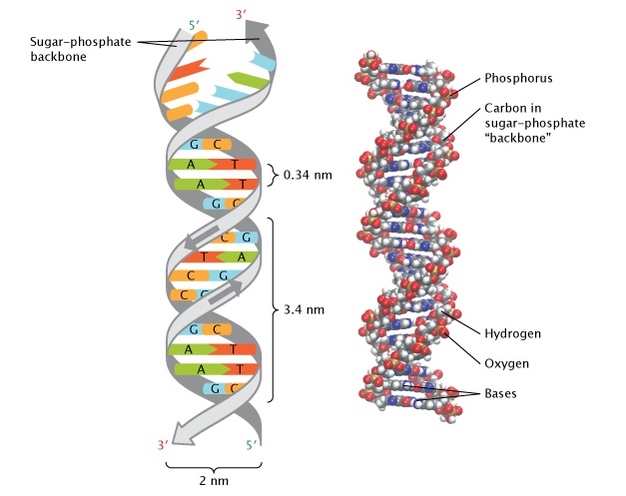
مثال دیگری از یک سوپرا مولکول، همان ساختار معروف DNA است. به تصویر زیر توجه کنید:
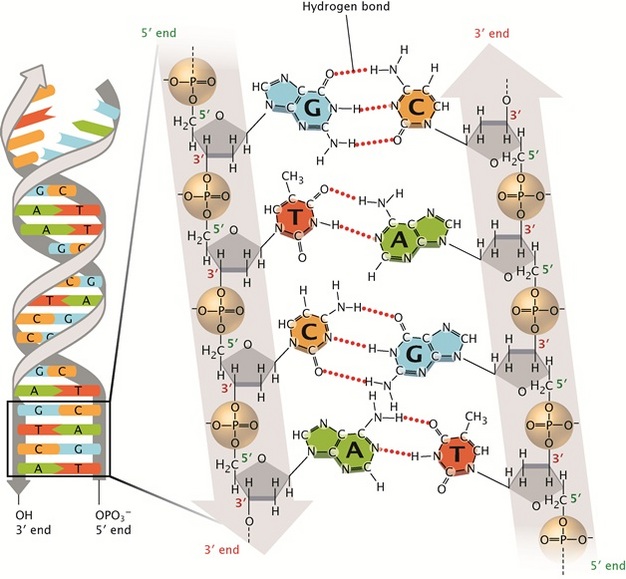
ما اینجا دو رشته داریم که بر روی هر یک از آن های باز های A, G, C و T قرار دارند؛ این باز ها با استفاده از پیوند های هیدروژنی به هم متصل شده اند و باعث شدند تا دو رشته DNA در کنار هم قرار بگیرد. در این تصویر پیوند های هیدروژنی به صورت نقطه چین های قرمز رنگ نشان داده شده اند.
در مثالی دیگر، در تصویر زیر ساختاری را مشاهده می کنید که اصطلاحا با آن کلاترات می گویند؛ این ساختار از کنار هم قرار گرفتن مولکول های آب ایجاد شده و در مرکز آن یک مولکول متان به دام افتاده است. در واقع، مولکول های آب، با ایجاد شبکه ای از پیوند های هیدروژنی، مانند قفسی به دور مولکول متان تجمع کرده اند.
در این مورد، نیرویی که باعث ایجاد ساختار شده، از نوع نیروی پراکندگی لاندن (london dispersion force) می باشد که در مقاله ای جداگانه به آن پرداخته ایم (برای مطالعه آن مقاله، اینجا کلیک کنید).
کاربرد شیمی سوپرامولکول
دانش سوپرا مولکول با توجه به تاریخ بسیار کوتاهی که دارد (بسیار نوین و جدید به حساب می آید) هنوز به صورت گسترده مورد استفاده قرار نگرفته، اما کاربرد هایی از آن را می توان دید که هم اکنون مورد استفاده است. به عنوان مثال، از برخی ساختار ها برای تکنیک های دارورسانی (drug delivery) استفاده می شود.
همچنین از برخی ساختار های دیگر، به عنوان کاتالیست استفاده شده است. جالب است بدانید که، یکی از پژوهش های صورت گرفته بر ساختار های سوپرا مولکول، تلاش هایی بوده که برای ساخت و شبیه سازی آنزیم ها انجام شده و نتیجه های بسیار موفقی نیز داشته است.
البته از آنجا که این شاخه از علم شیمی، هنوز چندان توسعه نیافته بنابراین بسیاری از کاربرد های آن، هم اکنون مشخص نیست و به تدریج و در طی سالیان آینده مشخص خواهد شد.